众所周知,骨关节炎的实质病变是关节软骨发生了退行性改变,出现了磨损,而关节软骨是无法再生的。因此,针对骨关节炎的传统治疗手段只能缓解,无法根治。
关节软骨是一种结构组成特殊的结缔组织,由于关节软骨内不含血管和神经系统,受到损伤后不具备自我修复能力。
而当前,针对早期至中期的骨关节炎主要治疗是姑息性干预措施,包括锻炼,减少重量,药物或注射。在姑息干预不足的中期和晚期骨关节炎的情况下,膝关节置换术等手术干预是最后的手段。然而,膝关节置换手术创伤大,还会引起感染,异物排斥等问题。因此,迫切需要开发新疗法以应对慢性膝关节疼痛。
随着再生医学技术的发展,干细胞凭借其多向分化,免疫调节,抗炎等特性在膝骨关节炎治疗中占据重要地位。

临床研究证实:间充质干细胞治疗骨关节炎具有三大益处
2021年2月,《International Orthopaedics》杂志上的一篇题为“Subchondral bone or intra-articular injection of bone marrow concentrate mesenchymal stem cells in bilateral knee osteoarthritis: what better postpone knee arthroplasty at fifteen years? A randomized study”的研究揭示:间充质干细胞注射到膝关节软骨下骨能够更好地稳定骨关节炎,从而延缓患者行全膝关节置换术的时间。

该研究纳入了骨关节炎分级相似的60名患者。将患者自体骨髓间充质干细胞浓缩物二等分,一份注入一侧股骨的软骨下骨,另一份注射入对侧膝关节内。定期随访,最终证实在骨关节炎患者的膝关节软骨下骨中植入间充质干细胞具有以下三大益处:
1)明显延长手术期限,减轻关节疼痛
2)软骨丧失及骨髓病变速度下降
3)软骨下骨注射更有效推迟手术时间
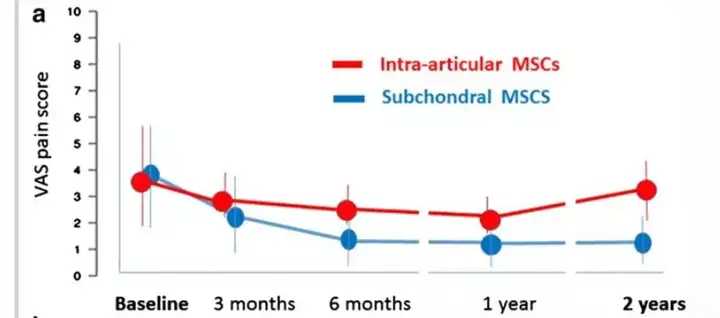
研究人员选取的60名患者双膝临床术前膝关节评分相似,均在52-55分左右(临床术前膝关节评分越高,则表明膝关节功能较好),疼痛评分相似。术后两年进行随访,数据显示:将间充质干细胞注射于软骨下骨的评分均在79分左右波动,而将间充质干细胞注射于关节炎的评分均在64分左右波动;此外,虽然患者疼痛评分也有所下降,但是通过软骨下注射的患侧膝盖较通过关节内注射的患侧膝盖疼痛评分下降趋势更明显,维持时间更持久。
通过对比前后影像学结果,发现:通过关节内注射的侧膝盖还是会出现关节间隙变窄的情况,但是通过软骨下注射的患侧膝盖却没有观察到这种情况;此外,用核磁共振测量软骨体积随时间改变时发现,通过关节内注射的侧膝盖软骨组织还是在不断减少,对比而来的是通过软骨下注射的患侧膝盖所测量到的软骨体积百分比增加。
更让人惊讶的是,通过软骨下注射的患侧膝盖骨髓病变有着明显的消退——从原先的2.9立方厘米消退至2.1立方厘米,但另一组却没有观察到这一现象。
综上,影像学结果直观、客观的让人们了解到软骨下骨注射间充质干细胞所取得的效果较关节内注射的效果更好。
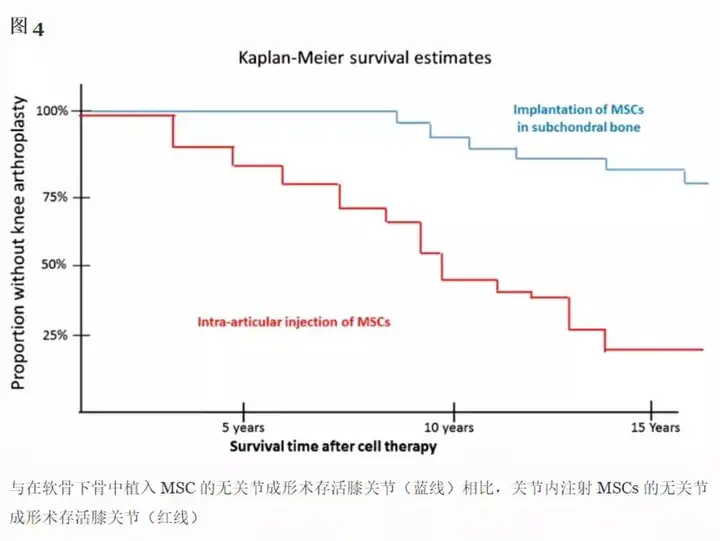
在术后15年的随访中,研究人员发现接受细胞疗法治疗的 120 膝中共有 54 例(45%)接受了全膝关节置换术 (TKA),该组的每年每膝关节置换术发生率为3%。在接受软骨下细胞治疗的 60 膝中,共有 12 膝(20%)接受了全膝关节置换;该组的每年每膝关节置换术发生率为 1.3%;对于接受关节内细胞治疗的 60 膝,共有42 膝(70%)接受了全膝关节置换术,其每年每膝关节置换术的发生率最高,为 4.6%。
综上所述,将间充质干细胞注射入软骨下骨可较好改善骨关节炎患者症状以及疾病情况,从而改善患者预后,延缓疾病进程,具有较好的研究前景。
干细胞技术治疗骨关节炎前景可期
2021年,中华医学会《中国骨关节炎诊治指南》中明确指出:目前全球已有超过3亿骨关节炎患者,而我国40岁以上人群原发性骨关节炎的总体患病率已高达46.3%。

干细胞作为一种具备高度分化能力的细胞,能够修复人体的各种组织。特别是对膝骨关节修复、软骨愈合及创伤后炎症等方面,它能在体内微环境作用下主动迁移至受损部位进行修复重建,促进受损的软骨重生。与此同时,它可以分泌多种具有调节免疫和抗炎作用的细胞因子,来缓解骨关节炎的临床症状,为从根本上治愈骨关节炎提供了可能。
而且根据国家药品监督管理局(NMPA)显示,目前共有3款针对膝骨关节炎的干细胞新药获得临床批件。此再次展示了干细胞在骨关节炎领域的临床应用前景。

随着干细胞技术的发展,干细胞治疗骨关节炎越来越被认为是一种极具前景的治疗方式。相信不久的将来,全球更多的骨关节炎患者将能够受益于干细胞技术。



